Как найти квантовые числа
- Квантовые числа: основные характеристики микроскопического мира
- Электронные уровни и квантовые числа
- Энергетические уровни и удаленность от ядра
- Орбитали и их характеристики
- Магнитное квантовое число и спин электрона
Квантовые числа: основные характеристики микроскопического мира
Квантовые числа играют важную роль в описании микроскопического мира. Они позволяют определить различные характеристики объектов таких, как электрон. Основным квантовым числом является число n, которое определяет энергию электрона. Формула для вычисления этой энергии: E = -13,6/(n^2) эВ, где n - натуральное число.
Электронные уровни и квантовые числа
Электронные уровни или электронные оболочки образуются, когда на многоэлектронных уровнях существуют электроны с одинаковым значением n. Каждому уровню соответствует буквенное обозначение A, B, C... в зависимости от значения квантового числа n. Максимальное количество электронов на уровне зависит от числа n и вычисляется по формуле: 2*(n^2).
Энергетические уровни и удаленность от ядра
Энергетический или электронный уровень представляет собой стационарное состояние электрона. Главное квантовое число характеризует удаленность электрона от ядра.
Орбитали и их характеристики
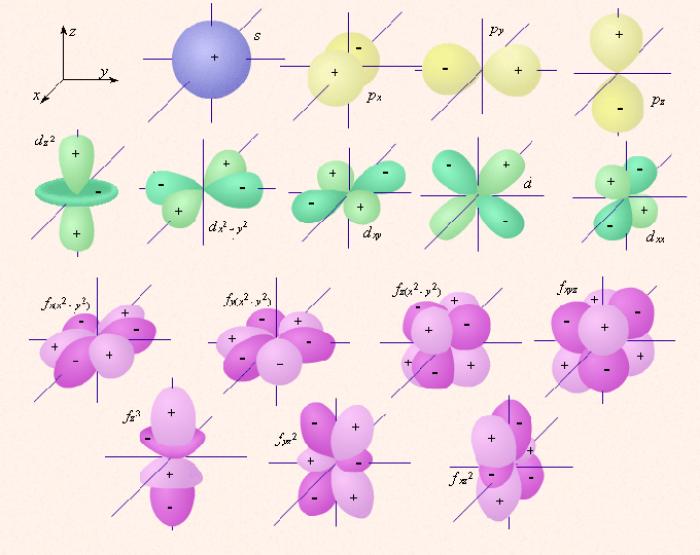
Квантовое число l, или орбитальное число, принимает значения от 0 до n-2 и характеризует форму орбиталей и подоболочку, на которой расположен электрон. Буквенные обозначения s, p, d, f, g... также присутствуют в записи электронной конфигурации химического элемента и определяют квантовое число. Количество электронов на подоболочке может быть до 2*(2l+1).
Магнитное квантовое число и спин электрона
Магнитное квантовое число ml определяет атомную орбиталь и принимает значения от 1 до -1. Спин электрона является важной характеристикой и равен ½. Квантовые числа ms представляют две проекции спина электрона на ось и принимают значения ½ и –½.
Таким образом, квантовые числа являются важными инструментами для описания микроскопического мира и определения различных характеристик электрона.
